はじめに
有機合成では、実験で合成した化合物がきれいな状態であることは少なく、基本的に他の化合物(溶媒、試薬、副生成物など)と混ざった状態です。そのため、分離精製を行うことが不可欠です。
本記事では、分離精製技術の一つである、「カラムクロマトグラフィー」について記載します。
カラムクロマトグラフィーとは
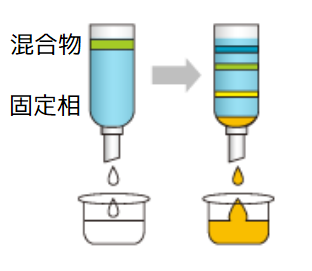
カラムクロマトグラフィーは、管の中にシリカゲルやアルミナなどの固定相を詰め、その固定相と、混合物中の各化合物との相互作用の違いにより分離する手法です。下図の左側が初期状態です。左の状態から移動相(=溶媒)を流していくと、固定相と混合物中の各物質の相互作用が異なるので、右側のように分かれていきます。
固定相(シリカゲル)-化合物間の相互作用
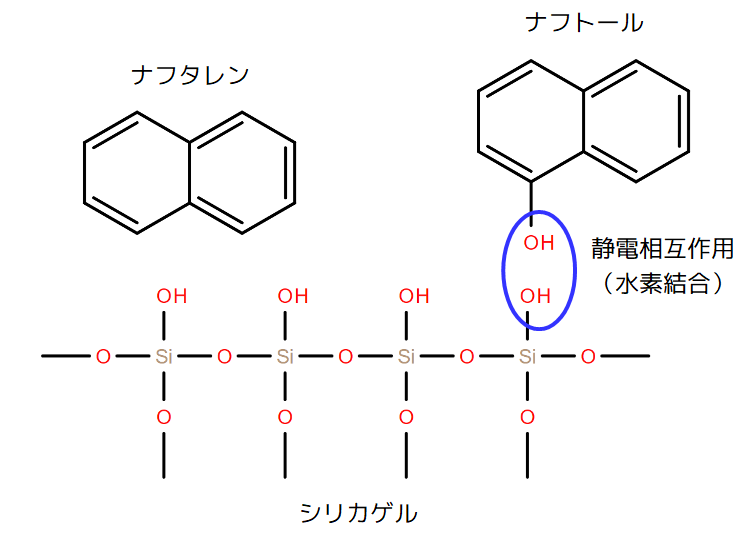
上記の相互作用として、シリカゲル($\ce{SiO2}$)を固定相に用いた場合の例を示します。化合物の例として、ナフタレンとナフトールを挙げました。ナフタレンはシリカゲルの$\ce{OH}$基と相互作用する官能基を持ちません。一方でナフトールは、自身の$\ce{OH}$基とシリカゲルの$\ce{OH}$基の間に静電相互作用が働きます。
この結果、ナフトールのほうがシリカゲルに強く固定され、カラムから出にくいということになります。
移動相の選択
ここまではシリカゲル-化合物間の相互作用のみを考慮しましたが、実際のカラムクロマトグラフィーでは移動相(溶媒)が流れています。この移動相の種類も重要です。カラムクロマトグラフィーでは、ヘキサンと酢酸エチルを用いることが多いですが、ヘキサンでは化合物との静電相互作用がなく、化合物を流す力が弱いです。しかし、酢酸エチルは化合物との静電相互作用があり、シリカゲルと化合物の結びつきを弱めることができます。
実際のカラムクロマトグラフィーでは、2種以上の溶媒を混ぜて、化合物を流しだす強さ(溶出力)を調節しながら進めることが多いです。
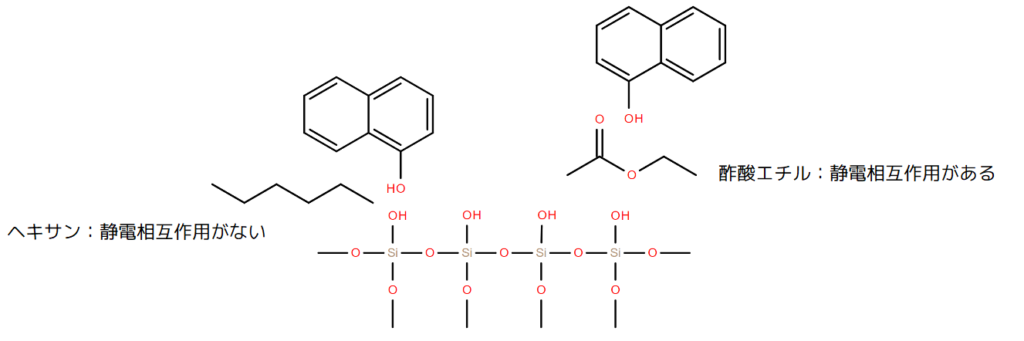
ヘキサンと酢酸エチルをシリカゲルカラムクロマトグラフィーで使う場合、酢酸エチルが多いほど溶出力が強くなります。
おわりに
本記事では、カラムクロマトグラフィーの簡単な原理を紹介しました。次回以降の記事で、実際に分離を行う際の判断などを書きたいと思います。


コメント